■状態変化は化学変化ではない
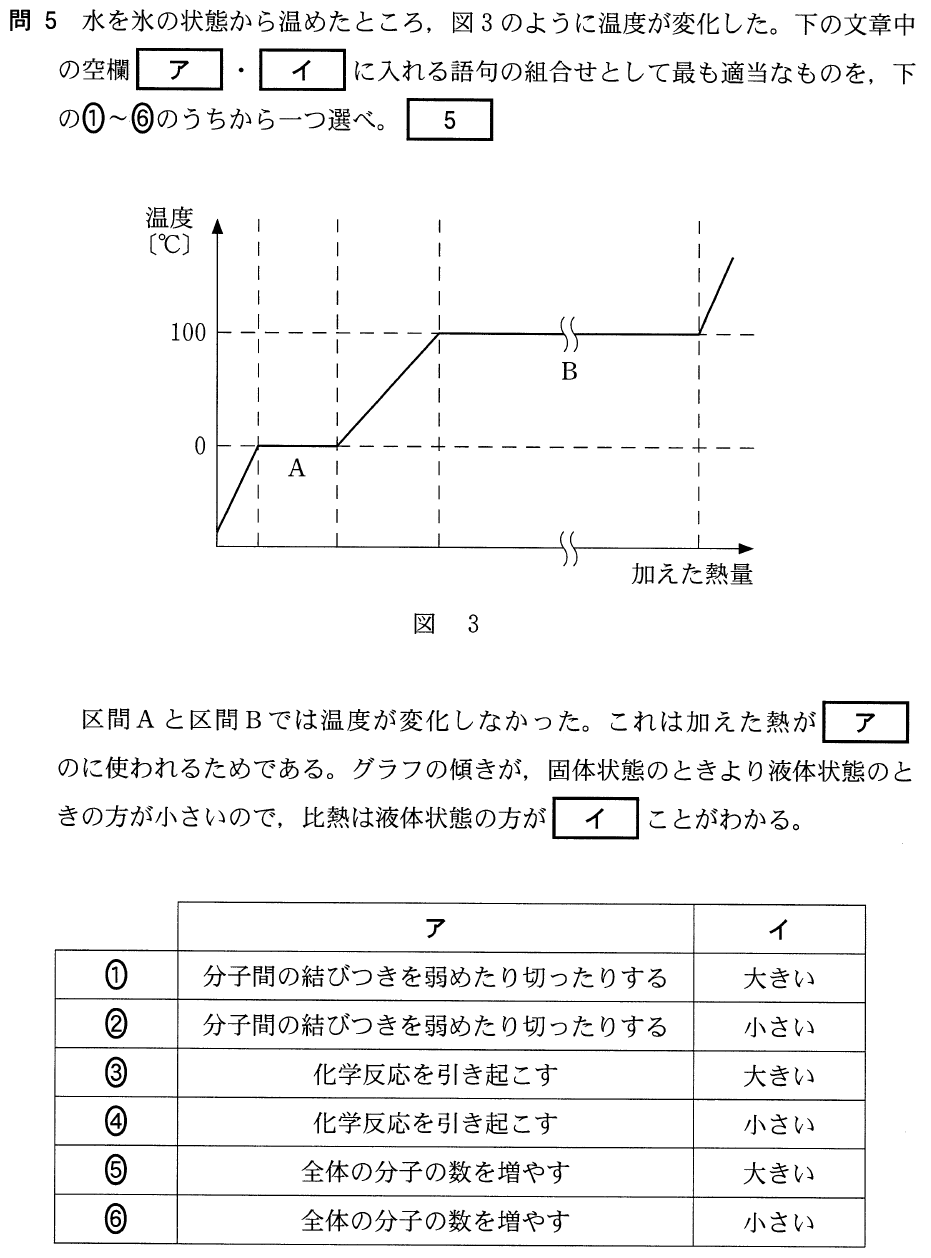
そうだね。最初の問題は熱を加えているにもかかわらず,区間Aや区間Bでは温度が上昇していないんだよね。その理由を選ぶんだね。
区間Aでは氷が水になって,区間Bでは水が水蒸気になっているのよね。
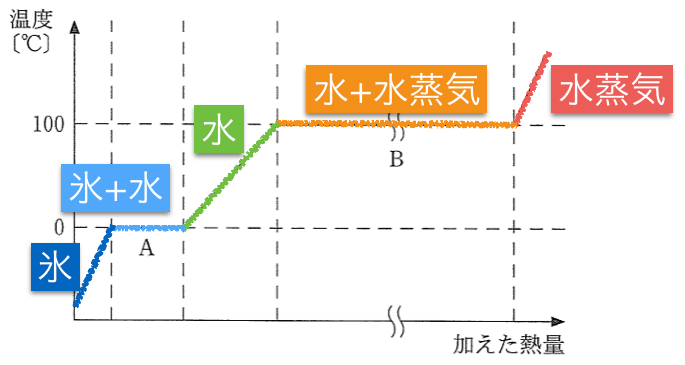
そうだね。「化学変化」では化学式が変わるんだけど,氷も水も水蒸気もH2Oだから,化学式が変わるわけではないね。つまり「化学変化」ではないね。
あと,全体の分子の数が増えているわけではないわよね。
ということは,温度が変化しない理由は「加えた熱量が分子間の結びつきを弱めたり切ったりするのに使われる」ということね。
■「比熱」の定義は大切!
そういうことだね。次の空欄はグラフの傾きと比熱の関係についてだね。そもそも「比熱」って何か分かる?
熱を加えたときの,温度の上がりやすさ,みたいな感じ?
比熱に関しては,できればきちんと説明ができるといいね。まぁ,説明できなくても,よく使う比熱を含む式が比熱を説明してくれているけどね。


■グラフの傾きが小さいほど比熱は大きい
この比熱の定義から,グラフの傾きと比熱の関係が分かるかな?
1gの物質があったとして,比熱が大きいということは,温度を1℃上昇させるのに必要な熱量が大きい,ということね。
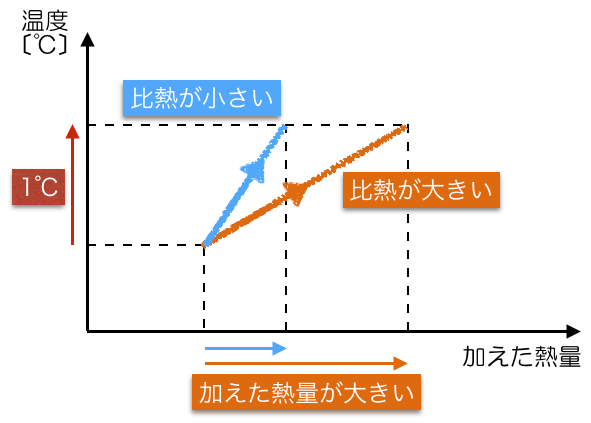
逆に同じ熱量を加えたとすると,比熱が大きいということは,温度の上がり方が小さいということになるわね。
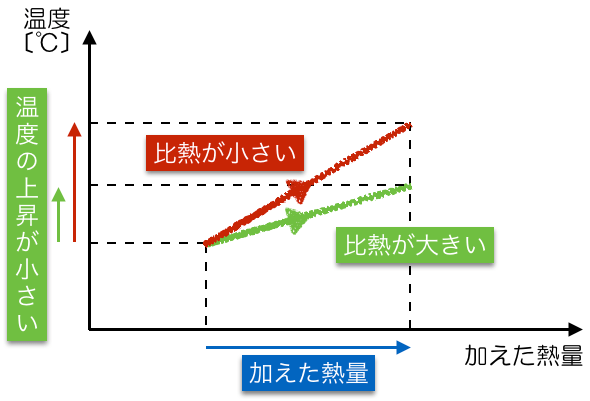
いずれにしても,このグラフでは,傾きが小さい方が比熱が大きいということになるわね。

その通りだ。ということは,グラフの傾きが液体状態のときの方が小さいので,比熱は大きいから,答えは①だね。ついでに式を変形して考えてみると,

グラフの傾きと比熱は反比例の関係にあるということね。








 センター試験の問題で「物理」を学ぼう!
センター試験の問題で「物理」を学ぼう!






